Senyawa Karbonil
Reaksi adisi organometalic.
 Uap dari Cairan Cadet 1760
Uap dari Cairan Cadet 1760
 Garam Zeize disintesis pada 1827 K[Pt(C2H4)Cl3] • H2O
Garam Zeize disintesis pada 1827 K[Pt(C2H4)Cl3] • H2O
 Grignard Reagents (XMgR)
Grignard Reagents (XMgR)
 1951 – 1952 Penemuan of ferrocene, Fe(h5-C5H5)2
1951 – 1952 Penemuan of ferrocene, Fe(h5-C5H5)2 Ziegler/Natta polymerization
Ziegler/Natta polymerization
 Kompleks Vaska
Kompleks Vaska
 Penemuan fulleren pada 1985
Penemuan fulleren pada 1985
Dalam kimia organik, gugus karbonil adalah sebuah gugus fungsi yang terdiri dari sebuahatom karbon yang berikatan rangkap dengan sebuah atom oksigen: C=O.
Istilah karbonil juga dapat merujuk padakarbon monoksida sebagai sebuah ligan pada senyawa anorganik atau kompleksorganologam (misalnya nikel karbonil); dalam situasi ini, karbon berikatan rangkap tiga dengan oksigen C≡O.
Sebuah gugus karbonil dikarakterisasikan oleh jenis-jenis senyawa berikut ini:
Senyawa karbonil lainnya termasuk urea dankarbamat. Contoh dari senyawa karbonil anorganik adalah karbon dioksida, karbon sulfida, dan fosgena.
Oksigen lebih elektronegatif daripada karbon, sehingga rapatan elektron akan tertarik dari karbon dan meningkatkan polaritas ikatan. Oleh karena itu, karbon karbonil bersifatelektrofilik, sehingga lebih reaktif terhadapnukleofil. Selain itu, oksigen yang elektronegatif juga dapat bereaksi dengan elektrofil.
Hidrogen alfa pada senyawa karbonil lebih asam (~1030 kali lebih asama) daripada ikatan CH yang biasa. Sebagai contoh, nilai pKa asetaldehida dan aseton adalah 16,7 dan 19, berturut-turut.[1]
Amida adalah penggandengan (coupling) karbonil yang paling stabil oleh karena stabilisasi resonansinya yang tinggi di antara ikatan Nitrogen-Karbon dengan Karbon-Oksigen.
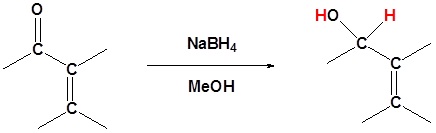
Gugus karbonil dapat direduksi oleh reagenhidrida seperti NaBH4 dan LiAlH4, dan oleh reagen organologam seperti organolitium danreagen Grignard.
Reaksi-reaksi penting lainnya meliputi:
- Reduksi Wolff-Kishner
- Reduksi Clemmensen
- Konversi menjadi tioasetal
- Hidrasi menjadi hemiasetal dan hemiketal, kemudian menjadi asetal dan ketal
- Reaksi dengan ammonia dan amina primer membentuk imina
- Reaksi dengan hidroksilamina membentukoksim
- Reaksi dengan anion sianida membentuksianohidrin
- Oksidasi dengan oksaziridina menjadiasiloin
- Reaksi dengan reagen Tebbe danfosfonium ilida menjadi alkena
- Reaksi Perkin
- Reaksi Tishchenko
- Kondensasi Aldol
- Reaksi Cannizzaro
Senyawa karbonil α,β-takjenuh adalah sebuah kelompok senyawa karbonil yang penting dengan struktur umumnya Cβ=Cα−C=O. Pada senyawa-senyawa ini, gugus karbonil berkonjugasi dengan sebuah alkena. Hal ini menyebabkan sifat-sifat khusus senyawa ini. Sebagai contoh senyawa ini adalah akrolein, mesitil oksida, asam akrilat, dan asam maleat. Karbonil takjenuh dapat dibuat dalam laboratorium menggunakanreaksi aldol dan reaksi Perkin.
Gugus karbonil, baik pada aldehida, asam, ataupun keton, menarik elektron dari alkena dan gugus alkena pada karbonil takjenuh, sehingga menurunkan reaktivitas terhadapelektrofil seperti bromin atau asam klorida. Sebagai kaidah umum, hidrogen melekatkan dirinya pada posisi alfa pada sebuah adisi elektrofilik. Sebaliknya, senyawa ini reaktif terhadap nukleofil pada adisi nukleofil.
Kimia Organologam telah dimulai sekitar jutaan tahun yang lalu.Cobalamin atau vitamin B12 merupakan senyawa organologam yang telah ada di alam, karena sudah ada di alam maka keberadaan senyawa organologam sudah ada sejak jutaan tahun yang lalu bahkan sebelum manusia ada.Dilakukan Total synthesis pertama terhadap Senyawa organologam pertama yaitu pada tahun 1972. Yang dimaksud Total sintesis yaitu mensintesis suatu senyawa dari sangat awal bagaikan merangkai atom per atom. Karena disintesis bagian perbagian maka senyawa cobalamin ini dibuat dalam waktu yang sangat lama, sekitar 20 Tahun
senyawa organologam pertama yang ditemukan oleh cadet pada tahun 1760. Namun senyawa organometal yang ia hasilkan bukanlah hasil yang diharapkan dari reaksi kalium asetat dan arsen trioksida . oleh karena itulah ada yang tidak setuju dengan pendapat bahwa cadet yang pertama mensintesis senyawa organometal.
Zeise menemukan senyawa organometal pertama yang memang disengaja. Setelah itu, Birnbaum mengkorfimasi adanya ligand H2C=CH2 pada1868 yang mendukung penemuan Zeise. Sedangkan pada 1975, struktur sempurna dari garam zeise terkarakterisasi sehingga membuktikan serangkaian penemuan dari terdahulunya
Grignard Reagents (XMgR) disintesis sekitar 1900 oleh victor Grignard Secara tak sengaja diproduksi ketika ingin membuat senyawa lain Saytzeff method. Saat itu ia sedang melakukan penelitian dibawah bimbingan dosennya bernama Barbier.
Keally, Pauson, dan Miller melaporkan synthesis ferrocene ini secara tak sengaja, karena sebenarnya mereka ingin mensintesis fulvalen. Yaitu senyawa sandwich hidrokarbon saja.
Ferrocene merupakan struktur yang sangat stabil dengan struktur 2 benzene yang mengapit atom Fe, karena sangat stabil maka penggunaan ferrocene ini sangat banyak. 1973 Nobel prize Geoffrey Wilkinson dan Ernst Otto Fischer karena banyak penelitiannya pada senyawa sandwich (metallocene).
1955 Ziegler dan Natta mengembangkan polimerisasi olefin pada tekanan rendah menggunakan campuran katalis logam (transition metal halide / AlR3)
Giulio Natta bekerja pada penelitian bersama Ziegler menerapkan a-olefin yang lain seperti propylene dan styrene pada reaksi polimerisasi. menghasilkan polypropylene dibuat menjadi 2 fraksi: amorphous (atactic) dan crystalline (tactic).pada 1963 Nobel prize untuk Karl Ziegler dan Giulio Natta pada katalis Ziegler-Natta yang nantinya digunakan secara komersil dalam pembuatan plastik
Pada tahun 1962 Kompleks Vaska dilaporkan oleh Lauri Vaska , senyawa ini memiliki kemampuan adisi oksidasi dan dapat mengikat O2 secara reversibel
Fulleren merupakan senyawa karbon yang saling berikatan membentuk suatu bentuk bola yang berongga. Fulleren ini dapat menangkap senyawa logam di dalamnya sehingga disebut juga metallofulleren.
Pengertian Senyawa Organologam
Senyawa kompleks organologam adalah senyawa kompleks yang memiliki ikatan logam-karbon antara satu sampai delapan atom karbon dalam ligan hidrokarbon terikat ke logam. Haptisitas mendeskripsikan jumlah atom dalam ligan yang mempunyai interaksi koordinatif dengan logamnya dan jumlah ini diberi simbol h (Huheey, 1993). Simbol h ini diikuti dengan superscriptyang menunjukkan jumlah atom ligan yang ditambahkan pada logam. Misalnya, ligan siklopentadienil dalam ikatan ferosen melalui kelima atomnya, sehingga menjadi h5-C5H5. Rumus kimia dari ferosen ditulis menjadi (h5-C5H5)2Fe (umumnya ligan hidrokarbon ditulis sebelum logamnya). Pengucapan dari penulisan ligan h5-C5H5 adalah ligan pentahaptosiklopentadienil (Miessler, 2003).
Senyawa kompleks organologam juga mempunyai suatu aturan dalam menghitung jumlah elektron sama seperti aturan oktet (aturan 8 elektron) pada kimia golongan utama. Aturannya adalah Aturan 18 Elektron. Aturan 18 elektron adalah aturan yang menghitung jumlah elektron valensi pada logam pusat yang berjumlah 18 elektron. Sama seperti halnya aturan oktet, aturan 18 elektron ini juga mempunyai banyak pengecualian. Namun, aturan ini masih dapat dijadikan pedoman untuk kompleks kimia organologam terutama ligan yang mengandung akseptor-π yang kuat (Miessler, 2003)
Sifat senyawa organologam yang umum ialah atom karbon yang lebih elektronegatif daripada kebanyakan logamnya. Senyawa komplek logam (biasanya logam-logam transisi) merupakan senyawa yang memiliki satu atau lebih ikatan logam-karbon. Senyawa organologam terdiri dari atom pusat dan ligan (Blaser et al, 2000).
Terdapat beberapa kecenderungan jenis-jenis ikatan yang terbentuk pada senyawaan organologam:
a. Senyawaan ionik dari logam elektropositif
Senyawaan organo dari logam yang relatif sangat elektropositif umumnya bersifat ionik, tidak larut dalam pelarut organik, dan sangat reaktif terhadap udara dan air. Senyawa ini terbentuk bila suatu radikal pada logam terikat pada logam dengan keelektropositifan yang sangat tinggi, misalnya logam alkali atau alkali tanah. Kestabilan dan kereaktifan senyawaan ionik ditentukan dalam satu bagian oleh kestabilan ion karbon. Garam logam ion-ion karbon yang kestabilannya diperkuat oleh delokalisasi elektron lebih stabil walaupun masih relatif reaktif. Adapun contoh gugus organik dalam garam-garaman tersebut seperti (C6H5)3C-Na+ dan (C5H5)2Ca2+.
b. Senyawaan yang memiliki ikatan -σ (sigma)
Senyawaan organologam dimana sisa organiknya terikat pada suatu atom logam dengan suatu ikatan yang digolongkan sebagai ikatan kovalen (walaupun masih ada karakter-karakter ionik dari senyawaan ini) yang dibentuk oleh kebanyakan logam dengan keelektropositifan yang relatif lebih rendah dari golongan pertama di atas.
Terdapat dua macam ikatan organologam, yaitu :
1. Ikatan ionik. Ikatan ionik organologam terbentuk dari unsur yang sangat elektropositif yaitu unsur pada golongan I, II, dan III. Organologam dengan yang berikatan secara ionik bersifat tak larut dalam pelarut hidrokarbon dan mudah teroksidasi.
2. Ikatan kovalen. Ikatan kovalen organologam yang mudah menguap terbentuk dari logam Zn, Cd, Hg, dan logam non-transisi gologan III (kecuali aluminium), IV, dan V. Ikatan kovalen ini terbentuk dengan cara memberikan satu elektron tunggalnya, baik dari logam maupun unsur organiknya, untuk dipakai secara bersama. Sifat dari senyawa organologam dengan ikatan kovalen ini mudah menguap, larut dalam pelarut organik, dan tidak larut dalam air.
Reaksi Grignard
Reaksi Grignard ditemukan oleh kimiawan Perancis Auguste Victor Grignard (1871-1935) di tahun 1901. Tahap awal reaksi adalah reaksi pembentukan metil magnesium iodida, reagen Grignard, dari reaksi antara alkil halida (metil iodida dalam contoh di bawah ini) dan magnesium dalam dietil eter kering.
CH3I + Mg –> CH3MgI
Anda pasti melihat bahwa magnisium terikat langsung dengan karbon. Senyawa semacam ini yang sering disebut sebagai reagen Grignard dengan ikatan C-logam dimasukkan dalam golongan senyawa organologam. Ikatan C-logam sangat labil dan mudah menghasilkan karbanion seperti CH3- setelah putusnya ikatan logam-karbon. Ion karbanion cenderung menyerang atom karbon bermuatan positif. Telah dikenal luas bahwa atom karbon gugus aldehida atau gugus keton bermuatan positif karena berikatan dengan atom oksigen yang elektronegatif. Atom karbon ini akan diserang oleh karbanion menghasilkan adduct yang akan menghasilkan alkohol sekunder dari aldehida atau alkohol tersier dari keton setelah hidrolisis.
C6H5CHO + CH3MgI –> C6H5CH(CH3)OMgI
Reaksi Grignard adalah contoh reaksi senyawa organologam. Karena berbagai jenis aldehida dan keton mudah didapat, berbagai senyawa organik dapat disintesis dengan bantuan reaksi Grignard.
Jenis-Jenis Senyawa Organologam
1. Alkil dan Aril Litium (Organolitium)
Senyawa Organolitium adalah senyawa Logam Alkali yang mempunyai sifat kelarutan dalam Hidrokarbon atau cairan nonpolar dan penguapan yang tinggi serta mempunyai sifat khas zat Kovalen. Penggabungan Molekular adalah suatu keistimewaan yang penting dari alkil baik dalam kristal maupun larutan. Jadi dalam Metil lithium atom-atom Li terletak pada sudut-sudut sebuah tetrahedron dengan gugus alkil berpusat pada bidang dihadapannya. Gugus CH3 secara simetris terikat pada tiga atom Li, dan ikatan jembatan alkil ini adalah dari jenis tuna elektron berpusat banyak.
Dalam larutan, sifat spesies terpolimerisasi bergantung pada pelarut, sifat sterik dari radikal organik dan suhu. Dalam Hidrokarbon MeLi, EtLi, n-PrLI, dan beberapa lainnya adalah heksamer, namun tert-butilitihium, yang tersolfasi. Tidak terdapat agregat yang lebih kecil dari pada tetramet. Meskipun demikian, bilamana digunakan pengkelatan amin ditersier, seperti tetrametiletilendiamen (TMED), Me2NCH2CH2NMe2 diperoleh kompleks alkillithium monomer yang stabil. Alkil dan aril juga membentuk kompleks dengan alkil logam lain seperti kompleks dengan Mg dan Zn. Sebagai contoh:
2LiC6H5 + Mg(C6H5)2→ Li2[Mg(C6H5)4]
Terdapat keragaman yang luas dalam kreaktifan perbandingan alkil, Li yang bergantung kepada perbedaan dalam agresasi dan interaksi pasangan ion. Suatu contoh adalah Bensinlitium, yang berupa monomer dalam tetrahidrofuran dan bereaksi dengan suatu supstrat tertentu lebih dari 104 kali lebih cepat dari pada metillithium tetramet. Kompleks TMED monomer yang disebutkan diatas juga lebih jauh dari reaktif dari pada agregat alkil yang bersangkutan. Alkillithium dapat mempolilithiasi asitilen,asetonitril, dan senyawa-senyawa lain, jadi CH3C≡≡ CH memberikan Li4C3, yang dapat dianggap sebagai turunan C34.
Reaksi alkil lithium umumnya dianggap bersifat sebagai ion karbon. Alkil alkena, khususnya Isoprena, yang memberikan sampai 90% 1,4-cis-polilisoprena, sebagai reaksi lainnya dengan alkena telah dipelajari kompleks TMED sekali lagi luar biasa aktif, tidak hanya berpolomerisasi etilena namun bahkan akan memelitisasi benzena dan senyawa aromatik, juga bereaksi dengan hidrogen pada 1 atm menghasilkan LiH dan alkana.
2. Senyawa Organo-Natrium dan Kalium
Semua senyawa ini benar-benar ionik dan tidak larut sampai batas apa pun dalam hidrokarbon karena sangat reaktif, peka terhadap udara, dan terhidrolisis kuat dalam air.
Yang terpenting adalah senyawa natrium dari hidrokarbon asam seperti siklopentadiena, idena, asitilena, dan sejenisnya. Ini diperoleh dari interaksi dengan logam natrium atau natrium yang dihamburkan dalam tetrahidrofuran atau dimetilformamida.
2CH5H6 + 2Na → 2C5H5-Na+ + H2
RC≡CH + Na → RC≡C-Na+ + ½ H2
3. Magnesium
Senyawa organik dari Ca,Sr, dan Ba sangat ionik dan relatif tidak berguna, namun senyawa magnesium mungkin adalah yang dipakai paling luas sebagai senyawa organik yang digunakan sangat luas dalam kimia organik dan dalam sintesis senyawa alkil dan aril dari unsur-unsur lain. Senyawa ini adalah jenis RMgX (pereaksi Grignard) dan MgR2. Yang pertama dibuat dengan interaksi langsung logam dengan suatu halida organik RX dalam suatu pelarut yang cocok, biasanya suatu eter seperti dietil eter atau tetrahidrofuran. Reaksinya biasanya paling cepat dalam iodida, RI, dan iod dapat digunakan sebagai suatu pengionisasi. Pereaksi RMgX digunakan in situ. Spesies MgR2 paling baik dibuat dengan reaksi kering.
HgR2 + Mg (berlebihan) →Hg + MgR2
Dialkil atau diaril kemudian diekstraksi dengan sutu pelarut organik. RMgX sebagai zat terlarut, maupun R2Mg adalah reaktif, dan menjadi peka terhadap oksidasi dengan udara dan terhadap hidrolisis dengan air.Sifat pereaksi Grignard dalam larutan adalah rumit dan bergantung pada sifat gugus-gugus alkil dan halida pada pelarut, konsentrasi dan suhu. Solvasi terjadi, dan penggabungan lebih utama terjadi dengan halida dari pada karbon berjembatan, kecuali bagi senyawa metil dimana jembatan oleh gugus CH3 terjadi.
Dalam larutan encer dan dalam pelarut donor yang lebih kuat, spesies monomer biasanya menonjol, namun dalam dietil eter pada konsentrasi yang lebih besar dari pada 0,1Mpenggabungan mmenghasilkan polimer linier atau siklis. Bagi pereaksi Grignard kristal, kedua struktur RMgX.nS dimana n adalah jumlah molekul pelarut, S, begantung pada sifat R, dan R(S)Mg(µ-X)2Mg(S)R telah ditemukan. Atom Mg biasaya terkoordinasi tetrahedral.
Senyawa seng dan kadmium mirip dengan senyawa magnesium namun berbeda dalam kereaktifannya. Alkil seng yang lebih rendah adalah cairan yang mudah menyalah dalam udara dan bereaksi kuat dalam air.
Reaksi Organologam
1. Insertion Reaction
Reaksi penyisipan merupakan suatu reaksi yang menyisipkan suatu molekul kedalam suatu senyawa organologam. Molekul yang menyisip kedalam senyawa organologam ini dapat bertindak sebagai 1,1 insertion dan 1,2 insertion, kedua hal ini merupakan suatu acuan bagaimana molekul ini menyisipkan dirinya diantara logam dan ligan senyawa organologam yaitu apakah menggunakan satu atom untuk mengikat logam dan ligan (1,1 insertion) atau molekul tersebut mempunyai dua atom yang satu mengikat logam sedangkan atom lain mengikat ligan (1,2 insertion). Contoh reaksi insertion dapat ditunjukan dari siklus reaksi dibawah ini (reaksi penyisipan di dalam kotak).
Pada reaksi diatas dapat dijelaskan bahwa senyawa HNi(CO)2Cl direaksikan dengan senyawa RCH=CH2 maka senyawa RCH=CH2 akan menyisip diantara logam dengan atom H. Reaksi ini merupakan 1,2 insertion, dimana ada dua atom C pada senyawa ini, satu atom C mengikat logam Ni dan atom C yang lain mengikat H, akibatnya ikatan rangkap pada molekul RCH=CH2 berubah menjadi tunggal karena elektronnya dipakai untuk mengikat logam dan atom H.
2. Carbonyl Insertion (Alkyl Migration)
Reaksi penyisipan karbonil pada dasarnya sama seperti penyisipan biasanya (1,1 insertion dan 1,2 insertion), tetapi yang membedakan disini adalah yang masuk diantara logam dan ligan adalah molekul karbonil (CO). Mekanisme reaksi dari penyisipan karbonil diusulkan ada tiga, yaitu penyisipan secara langsung, migrasi karbonil, dan migrasi alkil. Dari ketiga usulan mekanisme reaksi ini, dilakukan pengujian melalui eksperimental. Hasilnya mekanisme penyisipan karbonil yang diterima atau sesuai hasil pengujian adalah migrasi alkil. Jadi alkil bermigrasi dan terikat pada karbonil, tempat yang ditinggalkan alkil tadi ditempati karbonil dari luar. Contoh dari penyisipan karbonil diberikan pada siklus reaksi dibawah ini (dalam kotak):
Dari kedua gambar diatas, dapat dijelaskan bahwa reaksi penyisipan karbonil seperti dijelaskan pada pengantar singkat reaksi penyisipan karbonil diatas, mekanisme reaksinya adalah migrasi alkil. Pada gambar diatas ditunjukkan bahwa CH2CH2R bermigrasi ke CO, tempat kosong pada logam yang ditinggalkan alkil tersebut selanjutnya diisi oleh CO dari luar.
3. Hydride Elimination
Reaksi eliminasi hidrida ini yang sering ditemui adalah reaksi β-elimination yang merupakan suatu reaksi transfer atom H pada suatu ligan alkil (pada ligan posisi β terhadap logam) ke logam. Reaksi ini dapat menyebabkan meningkatnya bilangan oksidasi dan bilangan koordinasi dari logam. Proses transfer atom H pada alkil posisi β ini terjadi apabila posisi logam, carbon α, karbon β, dan hidrida koplanar. Contoh reaksi ini adalah pada siklus Wacker. Pada siklus ini terdapat reaksi β-hibrid-eliminasi (dalam kotak).
Pada reaksi diatas dinamakan reaksi β-hidrid-eliminasi karena pada molekul A, atom H yang terikat pada atom O (pada gugus OH posisi β terhadap logam), ditransfer menuju ke logam Pd. Pada contoh reaksi ini ternyata reaksi β-hidrid-eliminasi tidak hanya atom H milik alkil posisi β, tetapi dapat juga dari atom H dari gugus hidroksil (OH) pada posisi β. Atom H yang ditransfer ke logam Pd menyebabkan bilangan koordinasi logam Pd bertambah dari dua menjadi tiga. Hasil akhir dari reaksi ini adalah terbentuknya molekul B.
4. Abstraction Reaction
Reaksi abstraksi merupakan suatu reaksi eliminasi ligan yang tidak akan merubah bilangan koordinasi logam. Reaksi ini berkaitan dengan pembuangan substituent pada ligan dengan posisi karbon α dan β terhadap logam. Pembuangan substituent pada ligan ini dapat terjadi karena pengaruh suatu reagen eksternal. Contoh dari reaksi ini adalah:
Pada reaksi diatas (dalam kotak) disebut sebagai reaksi abstraksi dikarenakan terjadi pembuangan substituent yaitu atom H pada ligan η4-5-exo-RC5H5 (tetrahapto) yang disebabkan oleh reagen Ph3CPF6. Dari hasil pembuangan atom H ini, maka ligan η4-5-exo-RC5H5 berubah menjadi η5-RC5H4. Bilangan koordinasi logam pada reaksi ini tidak berubah, tetapi bilangan oksidasi logam Fe berubah dari Fe(0) menjadi Fe(II).
Reaksi reagen organometalik aldehid dan keton
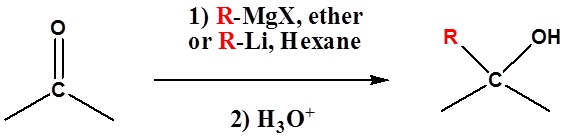
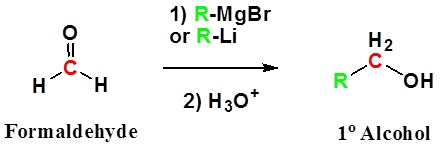
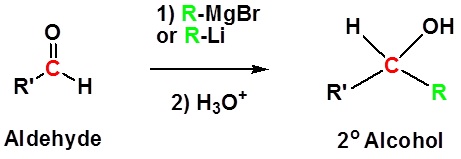
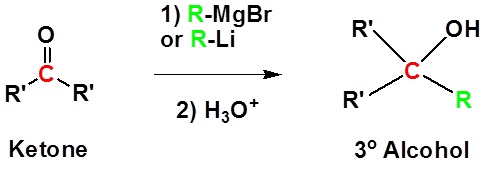
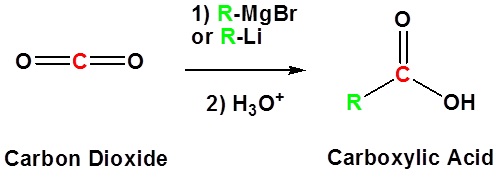
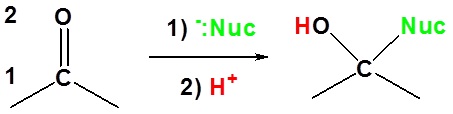
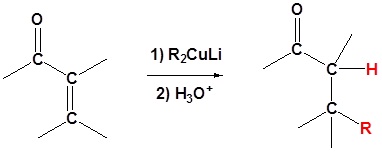
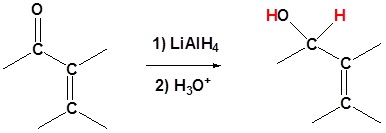
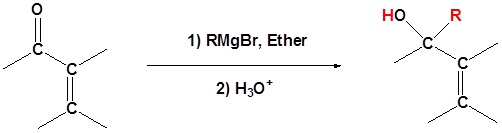
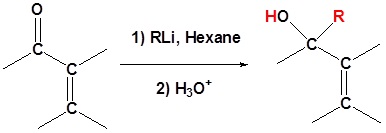
Permasalahan
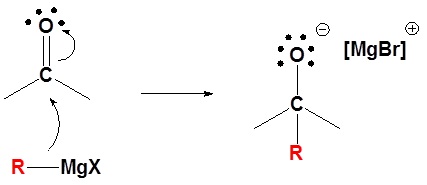
Karena reagen organologam bereaksi sebagai karbioninya, mereka adalah nukleofil yang sangat baik. Reaksi dasar melibatkan serangan nukleofilik karbon karbanionik dalam reagen organologam dengan karbon elektrofilik dalam karbonil untuk membentuk alkohol.
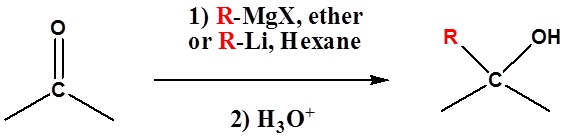
Baik Grignard dan Organolithium Reagen akan melakukan reaksi ini
Selain formaldehida memberikan alkohol 1o
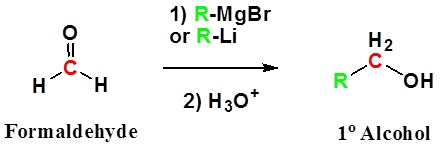
Selain aldehida memberikan 2 o alkohol
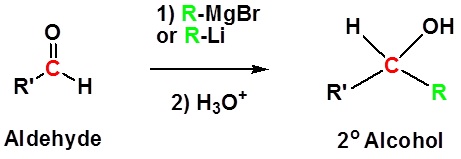
Selain keton memberikan 3o alkohol
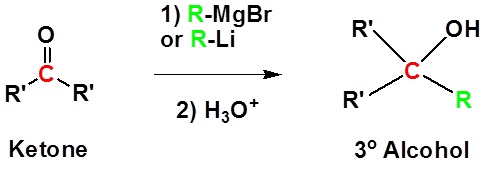
Penambahan karbon dioksida (CO 2 ) membentuk asam karboksilat
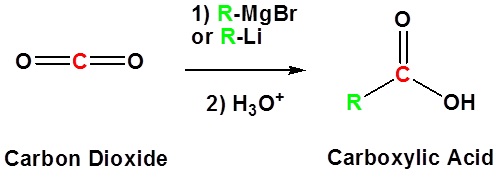
| Contoh |
|---|
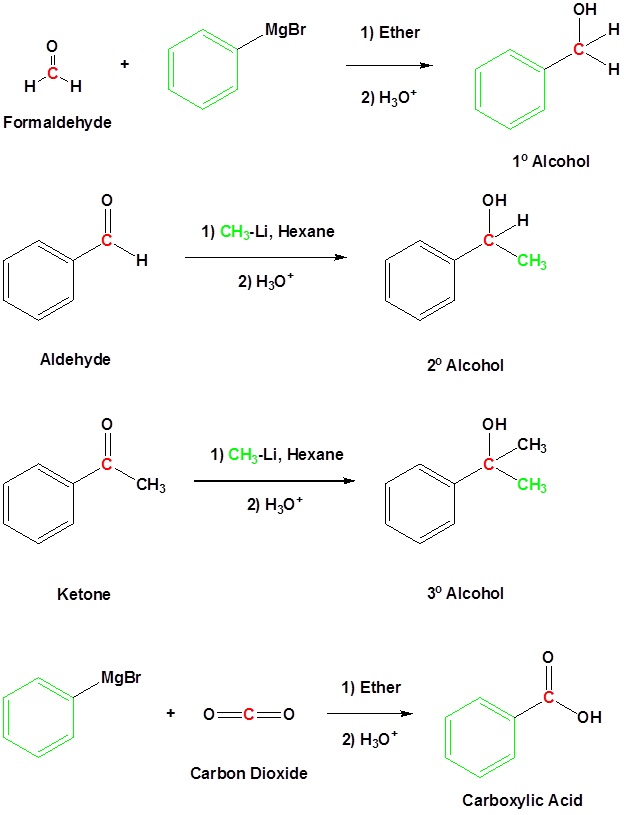 |
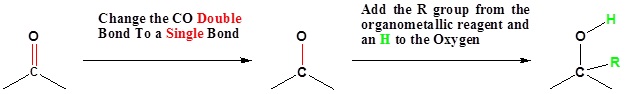
Pergi dari Reaktan ke Produk Sederhana

Mekanisme untuk Penambahan Karbonil
Mekanisme untuk agen Grignard ditampilkan.Mekanisme untuk reagen organologam adalah sama.
1) Serangan nukleofilik

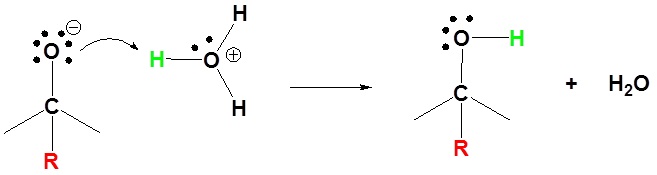
2) Protonasi

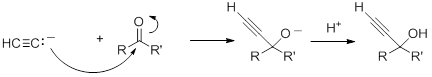
Penambahan Nukleofilik Asetilida ke Karbonil
Anion asetilid akan menambah aldehida dan ketonuntuk membentuk alkoksida , yang, setelah protonasi, memberikan propargil alkohol.

Dengan aldehid dan keton non-simetris, tanpa adanya katalis kiral, produk akan menjadi campuran rasemat dari dua enansiomer.
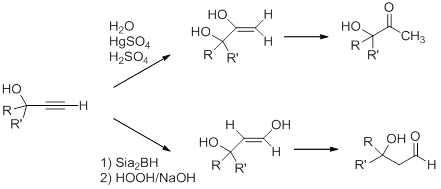
Ikatan rangkap tiga dalam alkohol propargil dapat dimodifikasi dengan menggunakan reaktivitas alkuna.Misalnya, Markovnikov dan anti-Markovnikov hidrasi ikatan rangkap tiga mengarah ke pembentukan keton dan aldehida yang tersubstitusi hidroksi, masing-masing, setelah enol-keto tautomerisasi .

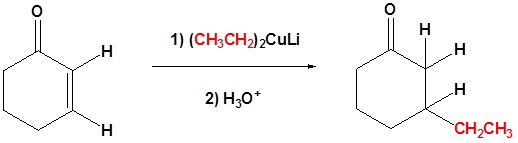
1,2- dan 1,4-Penambahan Pereaksi Organometalik
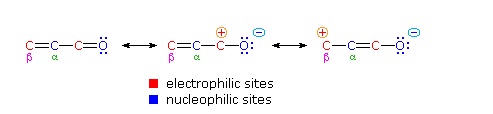
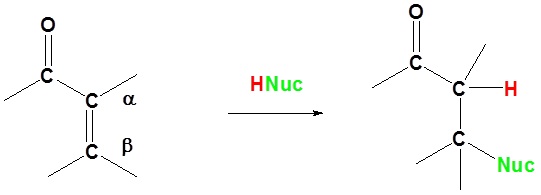
Salah satu kelas terbesar dan paling beragam dari reaksi terdiri dari penambahan nukleofilik pada gugus karbonil. Konjugasi ikatan ganda ke gugus karbonil mentransmisikan karakter elektrofilik karbon karbonil ke beta-karbon dari ikatan rangkap. Karbonil terkonjugasi ini disebut enones atau α, β karbonil tak jenuh. Deskripsi resonansi transmisi ini ditunjukkan di bawah ini.

Dari rumus ini harus jelas bahwa nukleofil dapat menyerang baik pada karbon karbonil, seperti untuk setiap aldehida, keton atau turunan asam karboksilat, atau pada beta-karbon. Kedua mode reaksi ini disebut sebagai 1,2-penambahan dan 1,4-penambahan masing-masing. A tambahan 1,4 juga disebut penambahan konjugasi.
Reaksi dasar penambahan 1,2
Di sini nukleofil menambah karbon yang ada di satu posisi. Hidrogen menambah oksigen yang ada di dua posisi.
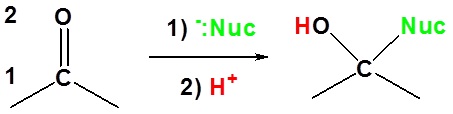
Reaksi dasar tambahan 1,4

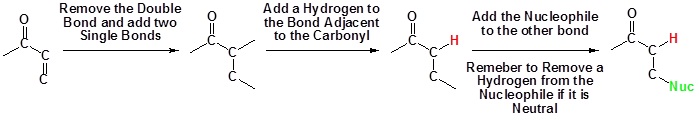
Dalam tambahan 1,4 Nucleophile ditambahkan ke karbon β ke karbonil sementara hidrogen ditambahkan ke karbon α ke karbonil.
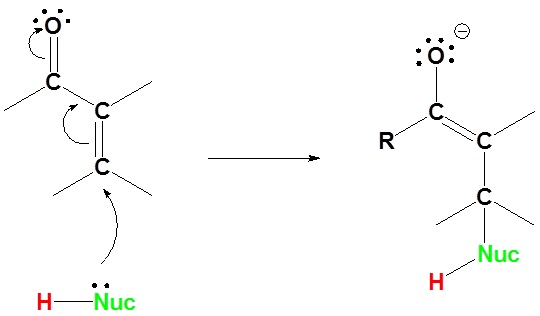
Mekanisme untuk penambahan 1,4
1) Serangan nukleofilik pada karbon β ke karbonil

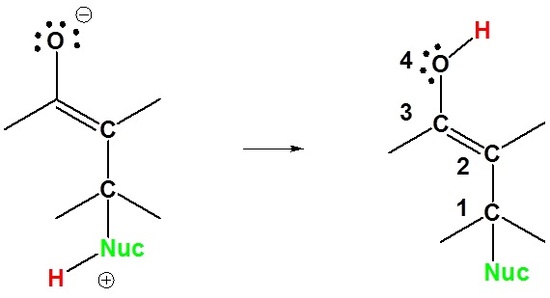
2) Transfer Proton

Di sini kita dapat melihat mengapa penambahan ini disebut 1,4. Ikatan nukleofil ke karbon dalam satu posisi dan hidrogen menambah oksigen dalam empat posisi.
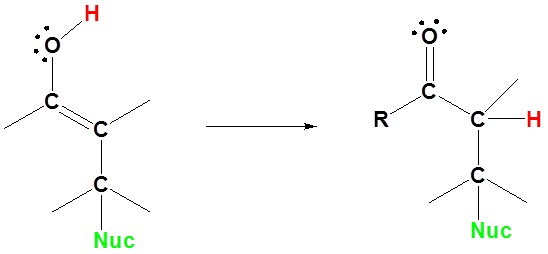
3) Tautomerisasi

Pergi dari reaktan ke produk disederhanakan

1,2 vs 1,4 kali
Apakah 1,2 atau 1,4-tambahan terjadi tergantung pada beberapa variabel tetapi sebagian besar ditentukan oleh sifat nukleofil. Selama penambahan nukleofil ada persaingan antara 1,2 dan 1,4 produk tambahan. Jika nukleofil adalah basa kuat, sepertireagen Grignard , reaksi 1,2 dan 1,4 tidak dapat diubah dan untuk itu berada di bawah kendali kinetik.Karena 1,2-tambahan pada gugus karbonil cepat, kita akan mengharapkan untuk menemukan keunggulan 1,2-produk dari reaksi-reaksi ini.
Jika nukleofil adalah basa lemah, seperti alkohol atau amina, maka penambahan 1,2 biasanya reversibel. Ini berarti persaingan antara 1,2 dan 1,4 tambahan berada di bawah kendali termodinamika. Dalam hal ini 1,4-penambahan mendominasi karena kelompok karbonil stabil dipertahankan.
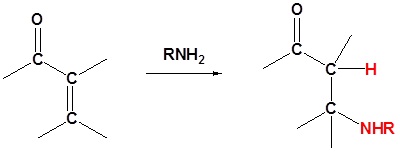
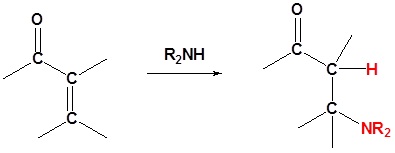
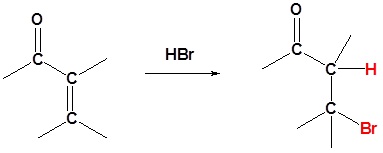
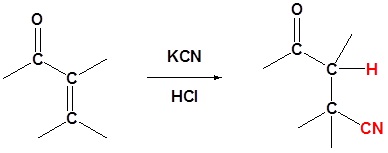
Nukleofil yang menambahkan 1,4 ke α, β karbonil tak jenuh
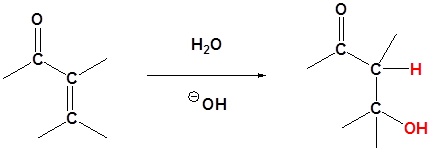
air

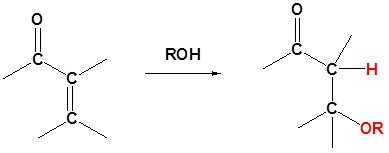
Alkohol

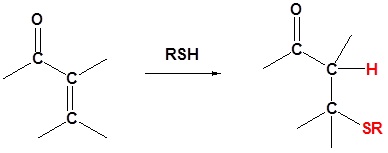
Thiols

1 o Amina

2 o Amina

HBr

Sianida

Gilman Reagen
Reaksi penting lainnya yang ditunjukkan oleh reagen organologam adalah pertukaran logam.Organolithium reagen bereaksi dengan iodida tembaga untuk memberikan pereaksi dimetilcopper litium, yang disebut sebagai reagen Gilman. Reagen Gilman adalah sumber carbanion seperti nukleofil yang mirip dengan reagen Grignard dan Organo lithium. Namun, reaktivitas reagen organocuprate sedikit berbeda dan perbedaan ini akan dieksploitasi dalam situasi yang berbeda. Dalam kasus α, β karbonat tak jenuh organocuprate reagen memungkinkan untuk penambahan 1,4 gugus alkil.Seperti yang akan kita lihat nanti, pereaksi Grignard dan Organolithium menambahkan gugus alkil 1,2 ke α, β karbonil tak jenuh
Organocuprate reagen terbuat dari reaksi reagen organolithium dan \ (CuI \)
\ [2 RLi + CuI \ rightarrow R_2CuLi + LiI \]
Ini bertindak sebagai sumber R: -
\ [2 CH_3Li + CuI \ rightarrow (CH_3) _2CuLi + LiI \]
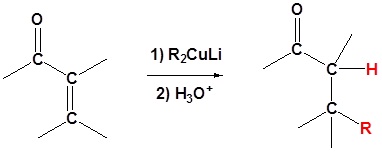
Contoh

Nukleofil yang menambah 1,2 menjadi α, β karbonil tak jenuh
Hidrida Logam
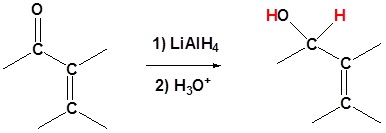

Reagen Grignard

Reagen Organolithium

Permasalahan
1. Dari artikel diatas, diakatakan bahwa anion asetilida akan menambah aldehida dan keton untuk membentuk alkoksida, yang setelah protonasi akan memberikan propargil alkohol. Dimana aldehida dan keton non simetris, tanpa adanya katalid kiral, maka produk akan menjadi campuran rasemat dari dua enansiomer. Bagaimana hal itu dapat terjadi?
2. Dari artikel diatas, diakatakan bahwa salah datu kelas terbesar dan paling beragam dari reaksi terdiri dari penambahan nukleofilik pada gugus karnobil. Dimana ada dua mode reaksi yang disebut sebagai reaksi dasar penambahan 1,2 dan reaksi penambahan 1,4. Apa yang membedakan terjadi nya reaksi tersebut dan reaksi mana yang akan mempertahakan kestabilan kelompok karbonil?
3. Dari artikel diatas, dikatakan bahwa reaksi penting lainnya yang ditunjukkan oleh reagen organologam adalah pertukaran logam. Organolitium reagen bereaksi dengan iodida tembaga untuk memberikan pereaksi dimetilcopper litium, yang disebut sebagai reagen gilman. Reagen gilman ini adalah sumber carbanion seperti nukleofil yang mirip dengan reagen grignard dan organolitium. Bagaimana perbedaan antara reagen gilman dan reagen grignard serta yang manakah yang paling efektif digunakan pada reaksi penambahan 1,4 ?























Saya akan menjawab pertanyaan ke 3 Reagen Gilman adalah sumber carbanion seperti nukleofil yang mirip dengan reagen Grignard dan Organo lithium. Namun, reaktivitas reagen organocuprate sedikit berbeda dan perbedaan ini akan dieksploitasi dalam situasi yang berbeda. Dalam kasus α, β karbonat tak jenuh organocuprate reagen memungkinkan untuk penambahan 1,4 gugus alkil.Seperti yang akan kita lihat nanti, pereaksi Grignard dan Organolithium menambahkan gugus alkil 1,2 ke α, β karbonil tak jenuh
BalasHapusOrganocuprate reagen terbuat dari reaksi reagen organolithium
Nomor 2 Reaksi penting lainnya yang ditunjukkan oleh reagen organologam adalah pertukaran logam.Organolithium reagen bereaksi dengan iodida tembaga untuk memberikan pereaksi dimetilcopper litium, yang disebut sebagai reagen Gilman. Reagen Gilman adalah sumber carbanion seperti nukleofil yang mirip dengan reagen Grignard dan Organo lithium. Namun, reaktivitas reagen organocuprate sedikit berbeda dan perbedaan ini akan dieksploitasi dalam situasi yang berbeda. Dalam kasus α, β karbonat tak jenuh organocuprate reagen memungkinkan untuk penambahan 1,4 gugus alkil.Seperti yang akan kita lihat nanti, pereaksi Grignard dan Organolithium menambahkan gugus alkil 1,2 ke α, β karbonil tak jenuh
BalasHapusSaya akan mencoba menjawab permasalahan no 1
BalasHapusAnion asetilid akan menambah aldehida dan ketonuntuk membentuk alkoksida , yang, setelah protonasi, memberikan propargil alkohol.
Dengan aldehid dan keton non-simetris, tanpa adanya katalis kiral, produk akan menjadi campuran rasemat dari dua enansiomer.
Ikatan rangkap tiga dalam alkohol propargil dapat dimodifikasi dengan menggunakan reaktivitas alkuna.Misalnya, Markovnikov dan anti-Markovnikov hidrasi ikatan rangkap tiga mengarah ke pembentukan keton dan aldehida yang tersubstitusi hidroksi, masing-masing, setelah enol-keto tautomerisasi .
Pertanyaan ke tiga
BalasHapusReaksi dari organolitium dan reagen Grignard mencerminkan karakter nukleofilik (dan dasar) dari karbon fungsional dalam senyawa ini. Banyak contoh reaksi tersebut akan ditemui dalam diskusi masa depan, dan lima contoh sederhana ditunjukkan di bawah ini.
Dengan aldehid dan keton non-simetris, tanpa adanya katalis kiral, produk akan menjadi campuran rasemat dari dua enansiomer.
BalasHapusIkatan rangkap tiga dalam alkohol propargil dapat dimodifikasi dengan menggunakan reaktivitas alkuna.Misalnya, Markovnikov dan anti-Markovnikov hidrasi ikatan rangkap tiga mengarah ke pembentukan keton dan aldehida yang tersubstitusi hidroksi, masing-masing, setelah enol-keto tautomerisasi .
Saya akan menjawab pertanyaan ke 3 Reagen Gilman adalah sumber carbanion seperti nukleofil yang mirip dengan reagen Grignard dan Organo lithium. Namun, reaktivitas reagen organocuprate sedikit berbeda dan perbedaan ini akan dieksploitasi dalam situasi yang berbeda. Dalam kasus α, β karbonat tak jenuh organocuprate reagen memungkinkan untuk penambahan 1,4 gugus alkil.Seperti yang akan kita lihat nanti, pereaksi Grignard dan Organolithium menambahkan gugus alkil 1,2 ke α, β karbonil tak jenuh
BalasHapusOrganocuprate reagen terbuat dari reaksi reagen organolithium
Saya akan menjawab pertanyaan ke 3 Reagen Gilman adalah sumber carbanion seperti nukleofil yang mirip dengan reagen Grignard dan Organo lithium. Namun, reaktivitas reagen organocuprate sedikit berbeda dan perbedaan ini akan dieksploitasi dalam situasi yang berbeda. Dalam kasus α, β karbonat tak jenuh organocuprate reagen memungkinkan untuk penambahan 1,4 gugus alkil.Seperti yang akan kita lihat nanti, pereaksi Grignard dan Organolithium menambahkan gugus alkil 1,2 ke α, β karbonil tak jenuh
BalasHapusOrganocuprate reagen terbuat dari reaksi reagen organolithium
No 2
BalasHapusReagen Gilman adalah sumber carbanion seperti nukleofil yang mirip dengan reagen Grignard dan Organo lithium. Namun, reaktivitas reagen organocuprate sedikit berbeda dan perbedaan ini akan dieksploitasi dalam situasi yang berbeda. Dalam kasus α, β karbonat tak jenuh organocuprate reagen memungkinkan untuk penambahan 1,4 gugus alkil.
Saya mencoba menjawab no 2 Reagen Gilman adalah sumber carbanion seperti nukleofil yang mirip dengan reagen Grignard dan Organo lithium. Namun, reaktivitas reagen organocuprate sedikit berbeda dan perbedaan ini akan dieksploitasi dalam situasi yang berbeda. Dalam kasus α, β karbonat tak jenuh organocuprate reagen memungkinkan untuk penambahan 1,4 gugus alkil.Seperti yang akan kita lihat nanti, pereaksi Grignard dan Organolithium menambahkan gugus alkil 1,2 ke α, β karbonil tak jenuh
BalasHapusPermasalahan 1 Ikatan rangkap tiga dalam alkohol propargil dapat dimodifikasi dengan menggunakan reaktivitas alkuna.
BalasHapusSaya akan mencoba menjawab permasalahan no 1
BalasHapusAnion asetilid akan menambah aldehida dan ketonuntuk membentuk alkoksida , yang, setelah protonasi, memberikan propargil alkohol.
Dengan aldehid dan keton non-simetris, tanpa adanya katalis kiral, produk akan menjadi campuran rasemat dari dua enansiomer.
Saya akan mencoba menjawab permasalahan no 1
BalasHapusAnion asetilid akan menambah aldehida dan ketonuntuk membentuk alkoksida , yang, setelah protonasi, memberikan propargil alkohol.
Dengan aldehid dan keton non-simetris, tanpa adanya katalis kiral, produk akan menjadi campuran rasemat dari dua enansiomer.
Saya akan menjawab no 2.
BalasHapusReagen Gilman adalah sumber carbanion seperti nukleofil yang mirip dengan reagen Grignard dan Organo lithium. Namun, reaktivitas reagen organocuprate sedikit berbeda dan perbedaan ini akan dieksploitasi dalam situasi yang berbeda. Dalam kasus α, β karbonat tak jenuh organocuprate reagen memungkinkan untuk penambahan 1,4 gugus alkil.Seperti yang akan kita lihat nanti, pereaksi Grignard dan Organolithium menambahkan gugus alkil 1,2 ke α, β karbonil tak jenuh